Spektroskopie ist im Kern eine sehr einfache Idee: Licht verrät, was in einer Quelle oder Probe passiert. Mal sieht man schmale Linien (typisch für Atome), mal breite »Berge« (typisch für Moleküle, Leuchtstoffe oder Fluoreszenz) und manchmal sogar Dellen, wenn Licht auf dem Weg »geschluckt« wird (Absorption).
Diese Übersichtsseite ordnet unsere Applikationsbeispiele deshalb nicht nach Quelle, sondern nach physikalischem Mechanismus. Das hilft Schüler:innen und Studierenden, beim Blick aufs Spektrum sofort die richtige Frage zu stellen: »Was erzeugt hier die Struktur — und warum?«
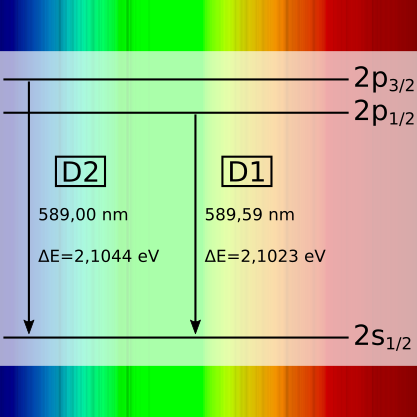
Grundidee: Elektrische Felder regen Atome/Ionen an ➙ beim Zurückfallen entstehen scharfe Linien bei ganz bestimmten Wellenlängen.
In Gasentladungen sind die Energieniveaus der Atome diskret – deshalb wirken die Spektren wie Barcode-Muster. Je nach Gasfüllung, Druck und »Betriebszustand« (kalt/warm) ändern sich Intensitäten und manchmal tauchen zusätzliche Linien auf. Ideal, um Kalibration, Linienzuordnung und »Welche Atome sind drin?« spielerisch zu üben.
Grundidee: Eine Entladung erzeugt (auch) UV ➙ ein Phosphor wandelt das in sichtbares Licht um ➙ im Spektrum: Linien + Bandemission.
Das ist die perfekte Brücke zwischen »Atom-Linien« und »breiten Hügeln«. Man sieht sehr anschaulich, dass Farbe nicht zwingend »direkt« aus der Gasentladung kommen muss, sondern oft über eine Umwandlungsschicht entsteht. Nebenbei lernt man Warm-up-Effekte (Startgaslinien vs. später dominierende Komponenten).
Grundidee: Licht kann auf dem Weg selektiv geschluckt werden – genau dort entstehen dann dunkle Linien oder »Einbrüche«.
Hier lernt man den vielleicht wichtigsten Perspektivwechsel: Strukturen im Spektrum sind nicht immer Emission. Absorption kann Linien aus einem Kontinuum herausstanzen (Sonne) oder sogar eine starke Emissionslinie »von innen heraus« eindellen (Self-reversal). Didaktisch super, weil es direkt zur Frage führt: »Wo sitzt der Absorber – und wie sieht der Lichtweg aus?«
Grundidee: Ein Stoff nimmt Anregungslicht auf (oft UV/Blau) und emittiert danach bei längerer Wellenlänge ➙ meist breite Emissionsbänder.
Fluoreszenz ist der Türöffner zu Molekül- und Festkörperphysik: vibronische Übergänge, Aktivator-Ionen, Defektzentren – alles wird plötzlich sichtbar. Und: Diese Experimente sind extrem »show-tauglich«, weil das Leuchten schon mit bloßem Auge beeindruckt, das Spektrum aber die Struktur dahinter erklärt.
Grundidee: Bei Chemolumineszenz entsteht Licht direkt in einer chemischen Reaktion. Die Reaktion erzeugt angeregte Moleküle (oder regt einen Farbstoff an), die beim Zurückfallen Licht emittieren – meist als breites Band statt schmaler Linien.
Das ist der »kalt leuchtende« Zweig der Spektroskopie: keine heiße Flamme, keine Gasentladung, kein Phosphor – nur Chemie, die Photonen produziert. Genau deshalb sind diese Spektren didaktisch so angenehm: Man erkennt schnell den Unterschied zwischen bandförmiger Molekülemission und linienförmiger Atomemission. Ideal als Einstieg, bevor es im nächsten Abschnitt »heiß« wird.
Grundidee: Bei Pyrotechnik liefert die Chemie zwar die Energie – das Licht entsteht aber in der heißen Flammen-/Plasma-Zone. Dort werden Atome und Moleküle angeregt, was zu Emissionslinien (z. B. Na, K, Cu …) und Molekülbanden (z. B. bestimmte Halogenid-/Oxid-Systeme) führt. Zusätzlich kann ein Kontinuum auftreten, wenn glühende Partikel mitstrahlen.
Das ist der »heiß leuchtende« Gegenpart zur Chemolumineszenz: Die Reaktion ist der Motor, aber das Spektrum ist das Protokoll dessen, was in der Flamme wirklich passiert. Genau hier wird Spektroskopie zum Rezeptdetektivspiel: Warum dominiert Gelb so oft (Na-D)? Wieso ist reines Blau so anspruchsvoll? Und wie unterscheiden sich Linien, Banden und Kontinuum in einem einzigen Messbild?
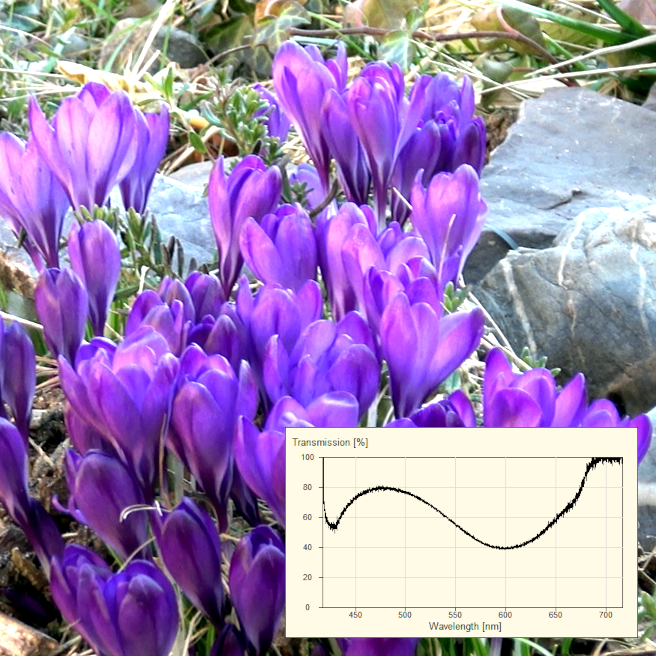
Grundidee: Weißes Licht durch eine Probe ➙ bestimmte Wellenlängen werden absorbiert ➙ das Transmissionsspektrum zeigt, welche Farben durchkommen.
Das ist der cleanste Einstieg in analytische Spektroskopie: Man misst nicht »Leuchten«, sondern »Filterwirkung«. Besonders cool wird’s, wenn sich die Molekülform ändert (pH-abhängig) und das Spektrum sichtbar wandert – exakt das, was Studis später als »Struktur ↔ Spektrum« wiedersehen.
Grundidee: In LEDs erzeugt Rekombination im Halbleiter Licht; bei Weißlicht-LEDs kommt oft Phosphor-Konversion dazu.
LEDs sind ideal, um »Spektrum als Designparameter« zu verstehen: Peaks (schmaler) vs. Phosphor-Berg (breiter), und bei Mehrkanal-Systemen sieht man direkt, wie Spektralkanäle gemischt werden. Das macht aus »Kelvin auf der Packung« eine physikalisch greifbare Kurve.
Grundidee: In der Praxis sind Lichtquellen gemischt (Gasentladung, Natriumdampf, LED …) – das Spektrum verrät die Technologie.
Draußen messen ist didaktisch Gold: Man verbindet Spektroskopie mit Umweltfragen (Lichtverschmutzung) und lernt, dass »gleiche Helligkeit« nicht »gleiches Spektrum« heißt. Gleichzeitig ist es ein schönes Setup-Beispiel (Messung auf Distanz).
Grundidee: Kombiniert man Lichtquellen, addieren sich ihre Spektren — perfekt für Kalibration und »Linien finden«.
Hier wird aus Spektroskopie ein Analyse-Spiel: Mehrere Laserdioden liefern sofort Referenzlinien (Grobkalibration), Überlagerung von LED+Laser zeigt »Spektren bauen«, und die »falsche Linie« trainiert echtes Auswerten statt Ablesen.
Hier können Sie unkompliziert eine Frage oder Anfrage zu unseren Produkten stellen:
Aktualisiert am: 23.03.2026